При поддержке
Задание №48211 ЕГЭ Химии
Условие задания #48211
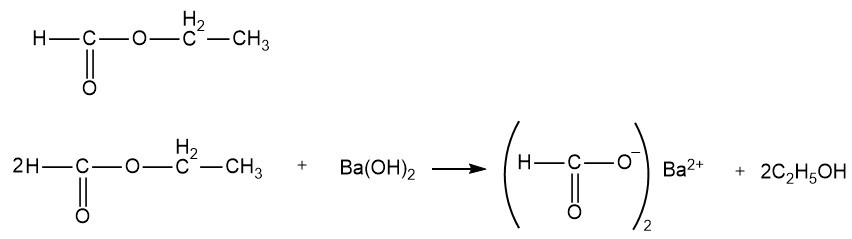
№33 по КИМПри полном сгорании органического вещества массой 51,8 г образовалось 47,04 л (при н. у.) углекислого газа и 37,8 г воды. Относительная плотность паров этого вещества по водороду равна 37. Установлено, что оно не реагирует с гидрокарбонатом калия, но взаимодействует со щелочами и аммиачным раствором оксида серебра. Установите молекулярную формулу вещества, изобразите его структурную формулу и напишите уравнение реакции с гидроксидом бария.
Похожие задания
15Решай задачи ЕГЭ в приложении
Скачивай наш Тренажер ЕГЭ на iPhone или Android и тренируйся в любое время и в любом месте!