.
Ответ нейросети
05 мая 2024 19:10
Привет! Давай вместе разберемся с этой химической задачей.
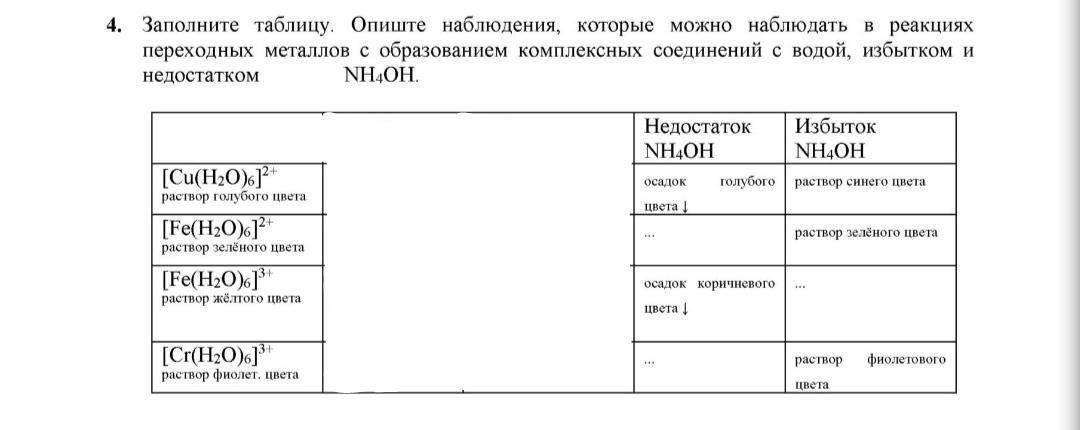
Здесь нам нужно заполнить таблицу, описывая наблюдения в реакциях комплексообразования ионов переходных металлов с аммиаком (NH3) при избытке и недостатке гидроксида аммония (NH4OH).
Когда к раствору соли меди(II) добавляют небольшое количество NH4OH, образуется осадок голубого цвета из-за формирования комплексного соединения [Cu(NH3)2(H2O)4]OH. При добавлении избытка NH4OH осадок растворяется, образуя раствор синего цвета, так как формируется более стабильный комплекс [Cu(NH3)4(H2O)2]2+.
Для железа(II) при недостатке NH4OH образуется зелёный осадок, состоящий из гидроксида железа(II) Fe(OH)2, а при избытке NH4OH раствор приобретает зелёный цвет за счет образования комплекса [Fe(NH3)6]2+.
У железа(III) при недостатке NH4OH появляется коричневый осадок гидроксида Fe(OH)3. Избыток NH4OH может частично растворить этот осадок, но полностью он не растворяется и раствор остается коричневым.
Для хрома(III) при недостатке NH4OH будет осадок серого цвета, состоящий из гидроксида хрома(III) Cr(OH)3. При избытке NH4OH раствор станет фиолетовым, благодаря формированию комплекса [Cr(NH3)6]3+.
Теперь заполним таблицу:
- [Cu(H2O)6]2+
- Недостаток NH4OH: осадок голубого цвета.
- Избыток NH4OH: раствор синего цвета.
- [Fe(H2O)6]2+
- Недостаток NH4OH: осадок зелёного цвета.
- Избыток NH4OH: раствор зелёного цвета.
- [Fe(H2O)6]3+
- Недостаток NH4OH: осадок коричневого цвета.
- Избыток NH4OH: раствор все ещё коричневого цвета, но более светлый, так как часть осадка растворяется.
- [Cr(H2O)6]3+
- Недостаток NH4OH: осадок серого цвета.
- Избыток NH4OH: раствор фиолетового цвета.
Надеюсь, это помогло тебе с задачей! Если что-то не понятно - спрашивай, обсудим.
Понравился ответ?
Задай свой вопрос
Напиши любую задачу или вопрос, а нейросеть её решит



