Привет! Давай разбираться с твоим вопросом. :)
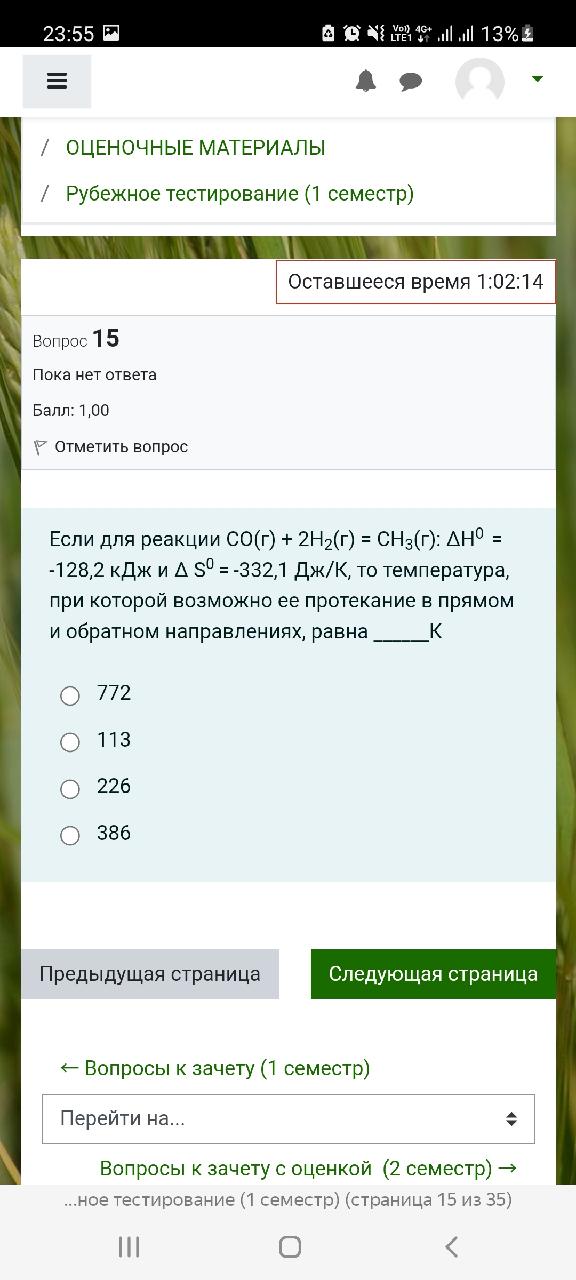
У нас есть уравнение для реакции ( SO(g) + 2H_2(g) = CH_3OH(g) ), для которой даны значения энтальпии (( \Delta H^0 = -128,2 ) кДж) и энтропии (( \Delta S^0 = -332,1 ) Дж/К).
Чтобы найти температуру, при которой реакция может идти в прямом и обратном направлениях (то есть, находится в равновесии), нужно использовать уравнение Гиббса:
[ \Delta G^0 = \Delta H^0 - T \Delta S^0 ]
При ( \Delta G^0 = 0 ) система находится в равновесии, и можно выразить температуру (( T )) равновесия из этого уравнения:
[ T = \frac{\Delta H^0}{\Delta S^0} ]
Как я уже сказал ранее, нам не следует использовать формулы в тестах, так что давайте сначала переведем значения к одной единице измерения. В данном случае переведём энтальпию из кДж в Дж:
[ -128,2 \text{ кДж} = -128200 \text{ Дж} ]
Теперь подставляем значения в формулу и получаем:
[ T = \frac{-128200 \text{ Дж}}{-332,1 \text{ Дж/К}} ]
Посчитаем:
[ T \approx \frac{-128200}{-332,1} \text{ К} ]
[ T \approx 386 \text{ К} ]
Так что правильный ответ - 386 K. Удачи на тесте!