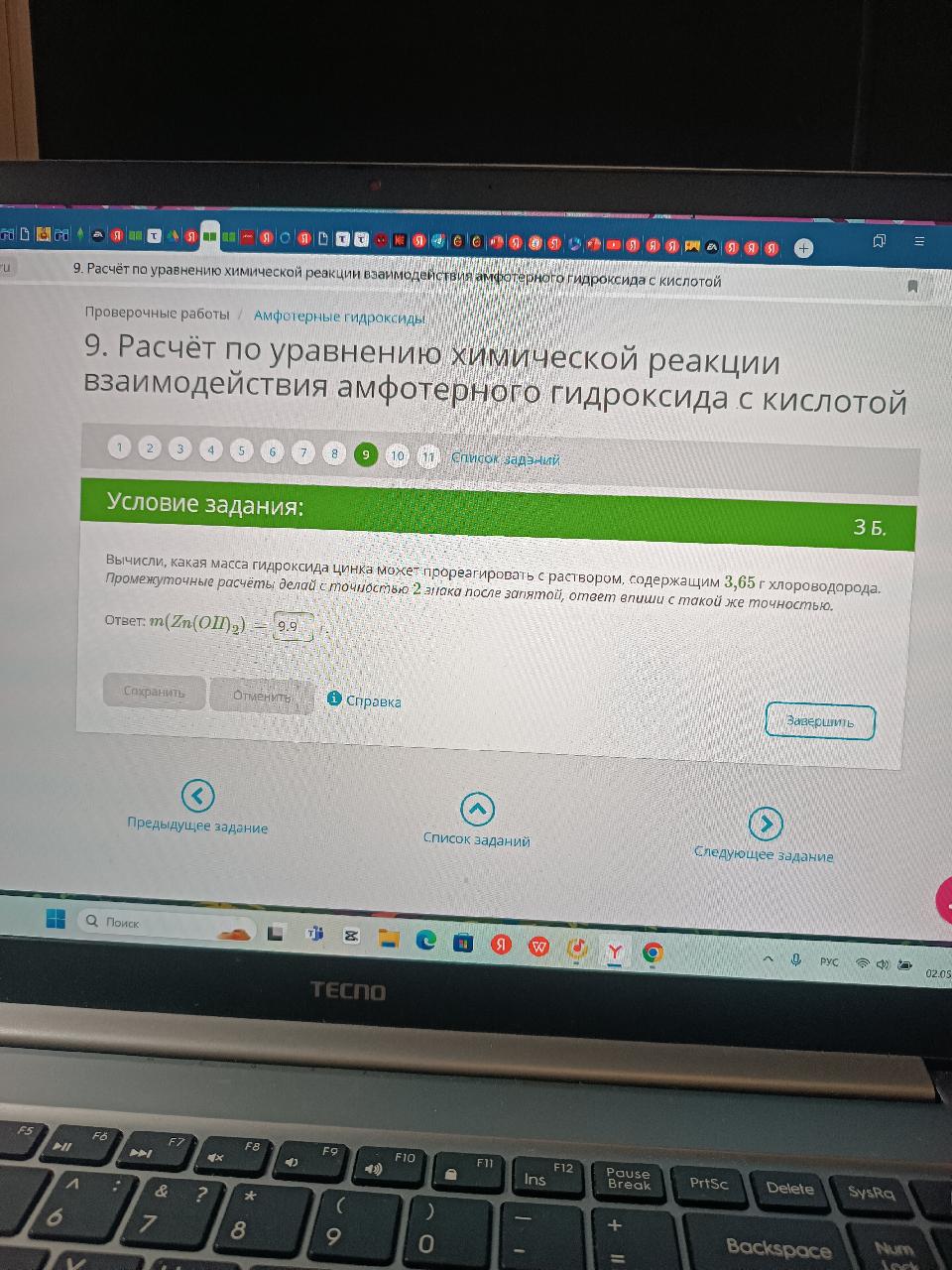
Хорошо, давай посмотрим на задачу. Тебе нужно вычислить массу гидроксида цинка, который может прореагировать с раствором, содержащим 3.65 грамма хлороводорода (HCl). Для решения этой задачи нам сначала нужно записать уравнение химической реакции между гидроксидом цинка (Zn(OH)2) и хлороводородной кислотой (HCl).
Уравнение реакции:
Zn(OH)2 + 2HCl → ZnCl2 + 2H2O
Теперь, когда у нас есть сбалансированное уравнение, можно приступать к расчетам. Начнем с определения молярной массы HCl. Молярная масса H (водорода) составляет приблизительно 1 г/моль, а Cl (хлора) — 35.5 г/моль. Сложим их, чтобы узнать молярную массу HCl:
1 (H) + 35.5 (Cl) = 36.5 г/моль
Теперь мы можем найти количество молей HCl, используя данные из задачи:
количество молей HCl = масса / молярная масса = 3.65 г / 36.5 г/моль ≈ 0.1 моль
Согласно уравнению реакции, 2 моля HCl реагируют с 1 молем Zn(OH)2. Таким образом, для реакции с 0.1 моля HCl потребуется:
0.1 моль HCl * (1 моль Zn(OH)2 / 2 моль HCl) = 0.05 моль Zn(OH)2
Теперь вычислим молярную массу Zn(OH)2:
Молярная масса Zn = 65.4 г/моль
Молярная масса O = 16 г/моль
Молярная масса H = 1 г/моль
Молярная масса Zn(OH)2 = 65.4 (Zn) + 2 * 16 (O) + 2 * 1 (H) = 65.4 + 32 + 2 = 99.4 г/моль
И теперь, чтобы найти массу Zn(OH)2, которая реагирует с 3.65 г HCl, умножаем количество молей Zn(OH)2 на его молярную массу:
масса Zn(OH)2 = количество молей * молярная масса = 0.05 моль * 99.4 г/моль = 4.97 г
Итак, масса гидроксида цинка, которая может прореагировать с 3.65 г хлороводорода, составляет примерно 4.97 г.